Segunda ley de la termodinámica
Para recordar ... :
“La distancia que separó el descubrimiento del fuego por frotamiento de la invención por Herón de Alejandría (hacia el año 120 antes de nuestra era) de una máquina en la que el escape de vapor de agua producía movimiento de rotación, se mide indudablemente por milenios. Y de nuevo tuvo que transcurrir aproximadamente dos mil años hasta que se construyó la primera máquina de vapor, el primer dispositivo que permitió convertir el calor en un movimiento mecánico verdaderamente utilizable”.
Procesos reversible y no reversible
Los procesos en la naturaleza pueden ser espontáneos o no. Los espontáneos se producen sin la intervención de agentes externos y los no espontáneo sí requiere la intervención de este tipo de agentes. Son ejemplos del primer grupo: la difusión entre dos sustancias, así como, la tendencia de los gases de ocupar todo e volumen que se les ofrece.
Los procesos espontáneos pueden se reversibles o no.
¿Qué diferencia existe entre los procesos reversibles y los irreversibles?
Procesos reversible | Procesos irreversible |
|---|---|
Los procesos reversibles son aquellos en que los sistemas pasan por los mismos estados de equilibrio por los que habían transitado anteriormente. | Los procesos que no cumplen con las condiciones anteriores se denominan irreversibles, pues no se mantiene el equilibrio termodinámico. Este es el caso de: el paso de calor de un cuerpo caliente a uno de menor temperatura. |
La irreversibilidad de los procesos en la naturaleza impone ciertos límites a la posibilidad de utilizar la energía interna para realizar trabajo en los motores térmicos los cuales se caracteriza por su rendimiento o eficiencia térmica.
Con este propósito el hombre ha creado las llamadas máquinas térmicas. Una de estas máquinas es la conocida máquina de vapor que desempeñó un importante papel en la revolución industrial.
Saber más : Sobre la máquina de vapor

Una máquina térmica es cualquier sistema capaz de convertir calor en trabajo mediante un proceso cíclico[1], donde el sistema retorna periódicamente a su estado inicial.
Toda máquina térmica posee una sustancia de trabajo (gas, líquido u otra) capaz de realizar trabajo sobre otro sistema a costa del calor absorbido. Por ejemplo:
En un motor de combustión interna, la sustancia de trabajo son los vapores de gasolina u otro combustible. En general, en este tipo de máquina se cumple que:
Estudio de caso : Reflexiona
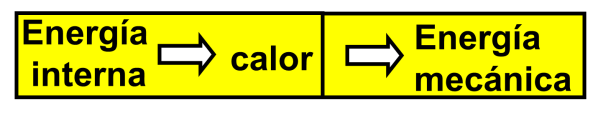
Cuando frotamos nuestras manos vigorosamente, el trabajo realizado provoca un incremento en la energía interna y un elevación de la temperatura. Cuando dejamos de frotarlas, las manos vuelven a su temperatura inicial. La energía térmica de las manos después de ser frotadas se transfiere al aire que las rodea, aunque no lo notemos. De acuerdo con la primera ley de la termodinámica, la energía mecánica se ha transformado en calor con una eficiencia de 100 %..
ΔQ = ΔW

¿Será posible convertir la energía térmica transferida al aire en trabajo con una eficiencia de 100%?
Si intentamos responder la pregunta anterior con el ejemplo presentado, nos encontraríamos que esto no es posible, pues no podemos capturar todo el calor transferido al aire y hacer que nuestras manos se froten.
: Segunda ley de la Termodinámica

Existen varios enunciados para la segunda ley de la termodinámica pero son análogos. Las dos formas más usadas de enunciarla, equivalentes entre sí, son:
Es imposible todo proceso cíclico[1] cuyo único resultado sea la transferencia de la energía en forma de calor de un cuerpo menos caliente a otro más caliente, es decir, es imposible hacer pasar el calor de un sistema más frío a otro más caliente en ausencia de otras variaciones simultáneas o en los cuerpos que los rodean.
Es imposible que ocurra un proceso periódico cuyo único resultado sea la obtención de trabajo a cuenta del calor tomado de una fuente (principio de Thomson).
Saber más :
Es imposible que ocurra un proceso periódico cuyo único resultado sea la obtención de trabajo a cuenta del calor tomado de una fuente (principio de Thomson). Es imposible todo proceso cíclico[1] cuyo único resultado sea la transformación de la energía en forma de calor de un cuerpo menos caliente a otro más caliente, es decir, es imposible hacer pasar el calor de un sistema más frío a otro más caliente en ausencia de otras variaciones simultáneas o en los cuerpos que los rodean ( R. Clausius[2]). Otra forma de enunciar la segunda ley de la termodinámica es la afirmación, deducida experimentalmente, de que es imposible construir un móvil perpetuo de segunda especie. Es decir, que no se puede construir un dispositivo de acción periódica, basado en la primera ley de la termodinámica, que realice trabajo a expensas del enfriamiento de una fuente de calor.
Aplicación práctica : Motores térmicos
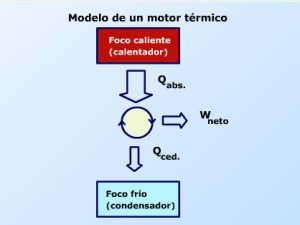
Ningún motor térmico puede funcionar si la temperatura de su agente de transformación es la misma que la del medio que lo rodea. Además si el foco frío (condensador) y el foco caliente (calentador) se encuentran en estado de equilibrio térmico, el motor térmico no puede realizar trabajo.
El motor térmico realiza trabajo a cuenta de la energía interna en el proceso de paso del calor de los cuerpos más calientes a los más fríos. En este caso el trabajo neto (total) realizado en cada ciclo (W) es siempre menor que la cantidad de calor (Q1 o Qabs.) que recibe el motor del cuerpo caliente (foco caliente FC). Parte del calor es absorbido (Q2 o Qced.) por el cuerpo más frío (foco frío FF).
Luego se cumple que: Q1= W + Q2 (Qabs.= W+Qced.)
Eficiencia de un motor térmico

Enlaces de interés
En los siguientes enlaces encontrarás información esencial para el estudio de las leyes o principios de la termodinámica[3].
Además podrás consultar algunos ejercicios resueltos y otras cuestiones de interés.
: Enlaces de interés

Segundo principio de la Termodinámica
En los siguientes enlaces encontrarás información esencial para el estudio de las leyes o principios de la termodinámica[3].
Además podrás consultar algunos ejercicios resueltos y otras cuestiones de interés.