Conceptos básicos
Masa de las moléculas

La masa de una molécula es muy pequeña y el trabajo práctico, en operaciones aritméticas, con su valor es muy difícil. Por ejemplo, en 1 g de agua hay 3,7·1022 moléculas, luego la masa de una molécula será aproximadamente de 3·10-26 kg. Por ello, no se trabaja con los valores absolutos de la masa, sino con valores relativos respecto a una sustancia tomada como referencia. Para ello se tomó como unidad 1/12 de la masa del carbono (de número atómico 12).
La masa molecular relativa es la suma de las masas atómicas relativas que la componen y que aparecen en la tabla periódica. Como por ejemplo la masa molecular relativa[1] del anhídrido (o dióxido) carbónico CO2 es aproximadamente igual a 44, ya que la masa atómica relativa del carbono es 12; y la del oxígeno es 16: 12+2·16=44.
La masa molecular relativa se denota como M(x), pero en la mayoría de los textos de Física se trata como µ, y su unidad de medida es g/mol. Además existe la unidad de masa atómica relativa (u), que antiguamente se denominaba como (u.m.a.), y que equivale a 1,66·10-27 kg.
También el tamaño de las moléculas es muy pequeño, si tenemos en cuenta el orden de magnitud de su masa. Para las moléculas de un solo átomo, monoatómicas, sus dimensiones son del orden de 10-8 cm. Las que poseen varios átomos son algo mayores pero aún siguen siendo pequeñas. Por ejemplo, la molécula de hidrógeno posee un tamaño aproximado de 2,3·10-8 cm. Si aumentamos el tamaño de esa molécula hasta que coincida con el de un bolígrafo, entonces el bolígrafo, con el mismo aumento, tendría un extremo en la Tierra y el otro en la Luna.

Cantidad de sustancia
Cuanto mayor sea el número de átomos o moléculas en los cuerpos, mayor es la cantidad de sustancia contenida en el cuerpo dado.
Definición : Cantidad de sustancia
Número relativo de átomos o moléculas que componen a un cuerpo dado. Se llama cantidad de sustancia a la relación entre el número de moléculas en el cuerpo y el número de átomos en 0,012 kg de carbono 12.
Es la razón entre el número de moléculas (N) contenidas en la muestra y el número de Avogadro (NA):
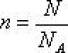
Unidad de medida es el mole.
El mole es igual a la cantidad de sustancia que contiene tantos átomos como hay 0,012kg de carbono 12.
Meditar :
Tenemos 3 moles de oxígeno ¿Qué significa esta expresión?
Indica que el número de moléculas en esa masa es 3 veces mayor que la que hay en 0,012 kg de carbono 12.
(La masa del mole de sustancia, medida en gramos, es numéricamente igual a su masa molecular relativa.
Esta magnitud denotada con la letra (n) y además se puede calcular como:
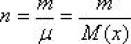
donde m es la masa de la sustancia (o gas) y µ o M(x) la masa molecular relativa de la sustancia.
Número de Avogadro
Teniendo en cuenta la propia definición de mole se deduce que:
No olvidar : Número de Avogadro
El número de moléculas (o átomos) que hay en un mole de sustancia es el mismo para todas las sustancias.
Número de Avogadro (NA )
6,02 · 1023 moléculas por mole
Mediante el número de moles de una sustancia (n) y el número de Avogadro (NA) podemos conocer la cantidad de moléculas (N) que hay en esa cantidad de sustancia con solo multiplicar ambas magnitudes: N = n · NA.
Velocidad de las moléculas
En toda cantidad de sustancia existe un número elevado de moléculas. Cada una de ellas se mueve con diferentes velocidades, pero la mayoría de las moléculas poseen velocidades cercanas a un cierto valor, llamado valor más probable. Generalmente se habla del término velocidad media cuadrática y a su raíz cuadrada se le conoce como velocidad cuadrática media .
Los experimentos fundamentales, sobre la distribución de las velocidades de las moléculas, fueron desarrolladas por Otto Stern[2] en 1920, y comprobaron las predicciones teóricas formuladas por James C. Maxwell[3] y Ludwig Boltzman[4].
: Actividad
Consulta el siguiente enlace donde encontrarás elementos que te ayudarán a profundizar en este tema y podrás consultar algunos ejercicios resueltos.
