Masa atómica relativa del oxígeno y de los elementos químicos
En la composición de los átomos de oxígeno podemos encontrar tres núcleos diferentes, en la que cada núcleo tiene igual número de protones (8) y diferentes números de neutrones (8, 9,10) respectivamente, con ocho electrones en los tres casos distribuidos en dos niveles de energía.
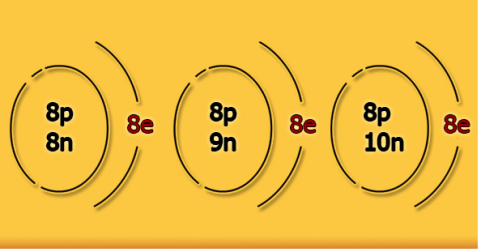
Definición :
Los átomos de un elemento que tienen igual número de protones y diferente número de neutrones reciben el nombre de isótopos.
La mayoría de los elementos químicos son una mezcla de isótopos naturales. Ejemplos:

Si se calcula la masa promedio de los tres isótopos del elemento oxígeno, teniendo en cuenta su abundancia relativa en la naturaleza, se conoce que esta es de 2,656 81. 10 -26 Kg. Comparando este valor con la masa de la unidad de masa atómica[1] que es de 1,66057 .10 -27 Kg se obtiene la masa atómica relativa del elemento químico oxígeno que se simboliza por Ar (O).
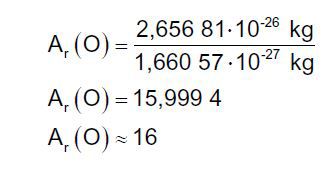
De manera similar, se han calculado y obtenido las masas atómicas relativas para cada elemento químico que se refleja en la tabla periódica.
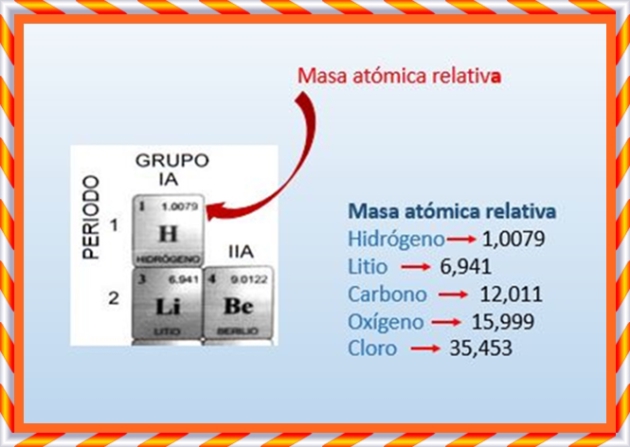
Recuerda que... : masa atómica relativa
La masa atómica relativa de cualquier elemento Ar (X), indica cuántas veces es mayor la masa de un elemento químico que la unidad de masa atómica.