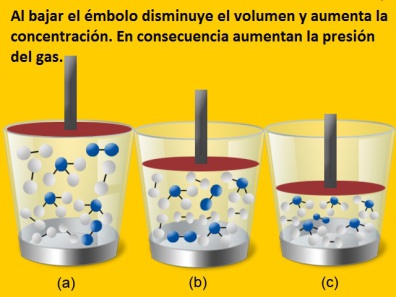
Presión de un gas. Presión atmosférica
Una importante característica que distingue a los fluidos de los sólidos es la presión. En los sólidos, al aplicar una fuerza sobre un sólido, el área sobre la cual está distribuida en muchas ocasiones puede no tenerse en cuenta, sin embargo determina en la presión que ejerce el cuerpo.
Estudio de caso : Presión en los sólidos
La presión que ejerce un bloque sobre la arena varía según el lado sobre el que se apoya.
NOTA: Accionando la lupita sobre la imagen esta se amplía y podrás observar mejor la diferencia.
La presión en los sólidos depende de la fuerza aplicada, en este caso el peso del bloque y del área de apoyo. Mientras menor es el área de apoyo , mayor es la presión que ejerce el bloque sobre el apoyo.
La presión caracteriza la fuerza distribuida sobre determinada superficie, ejercida perpendicularmente a dicha superficie.
Se calcula:
En el Sistema Internacional de unidades, la unidad fundamental de presión es:
Presión en líquidos y gases
Los líquidos y los gases se conocen como fluidos porque fluyen libremente y, a diferencia de los sólidos, tienden a adaptarse a la forma del recipiente que los contiene. Una propiedad que distingue a los líquidos y gases de los sólidos, es que se desplazan dejando lugar a los cuerpos que se hunden en ellos, envolviéndolos completamente. Esto origina una presión sobre dichos cuerpos.

: Presión de un gas
Los gases ejercen presión sobre las paredes del recipiente que los contienen.
Los choques individuales de las partículas con las paredes del recipiente son débiles, pero como el número de partículas en un pequeño volumen de gas es enorme, la cantidad de choques es suficiente para que se produzca una acción considerable sobre las paredes. Esta acción constituye la presión del gas.
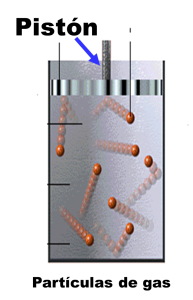
¿De qué depende que la presión que ejerce el gas sobre las paredes del recipiente, aumente?
Si en un recipiente que contiene gas echamos más gas, aumentará la presión.
La presión que ejerce el gas:
aumenta si aumenta la concentración de las partículas
manteniendo la temperatura constante, la presión del gas aumenta, si disminuye el volumen del recipiente que las contiene.
Fundamental :
A temperatura constante la relación entre el volumen y la presión del gas son inversamente proporcionales. Si se reduce el volumen del gas, la concentración de las partículas aumenta, porque disminuyen las separaciones entre ellas, aumenta el número de choques entre estas y contra las paredes del recipiente y aumenta la presión del gas.